
Alkalinitet utgör ett mått på vattnets buffringsförmåga, vilket är av stor betydelse för vattnets pH-värde och därmed för andra ämnens förekomstformer och löslighet. Vattnets alkalinitet utgörs huvudsakligen av vätekarbonatjoner (HCO3–).
Under framför allt senare halvan av 1900-talet har hela Sverige utsatts för nedfall av försurande svavel- och kväveföreningar [1]–[6]. Depositionen har varit störst i sydvästra Sverige.
En stor del av tillskottet av sura ämnen har neutraliserats genom att sulfat har fastlagts i marken och genom jonbyte där vätejoner har ersatt baskatjoner, främst kalcium och magnesium, på markpartiklarna. Marken har försurats medan grundvattnet ofta har skonats från pH-sänkningar och lägre alkalinitet. Markens kapacitet att genom dessa processer neutralisera syra är emellertid begränsad, och i ett längre tidsperspektiv är vittring av mineral av avgörande betydelse för att bevara stabila pH-värden i vattnet. Vid vittring av mineral produceras alkalinitet och baskatjoner.
I områden där marken inte längre erbjuder något försurningsskydd tas vattnets buffert av alkalinitet i anspråk. Alkaliniteten minskar i grundvattnet till en nivå där också pH-värdet börjar sjunka. Motståndskraften mot försurning bestäms alltså till stor del av hur lättvittrade mineralen i jordlager och berggrund är. I områden med svårvittrade jord- och bergarter (det vill säga utan karbonatmineral) ökar vittringen endast obetydligt vid lägre pH. I grundvattnet kan vittringskapaciteten direkt avläsas i alkaliniteten. I svårvittrade områden är vattnen jonsvaga med låg alkalinitet.
En mer utförlig beskrivning av försurnings- och neutralisationsprocesser finns i tidigare publicerade Bedömningsgrunder för grundvatten [7], [8].
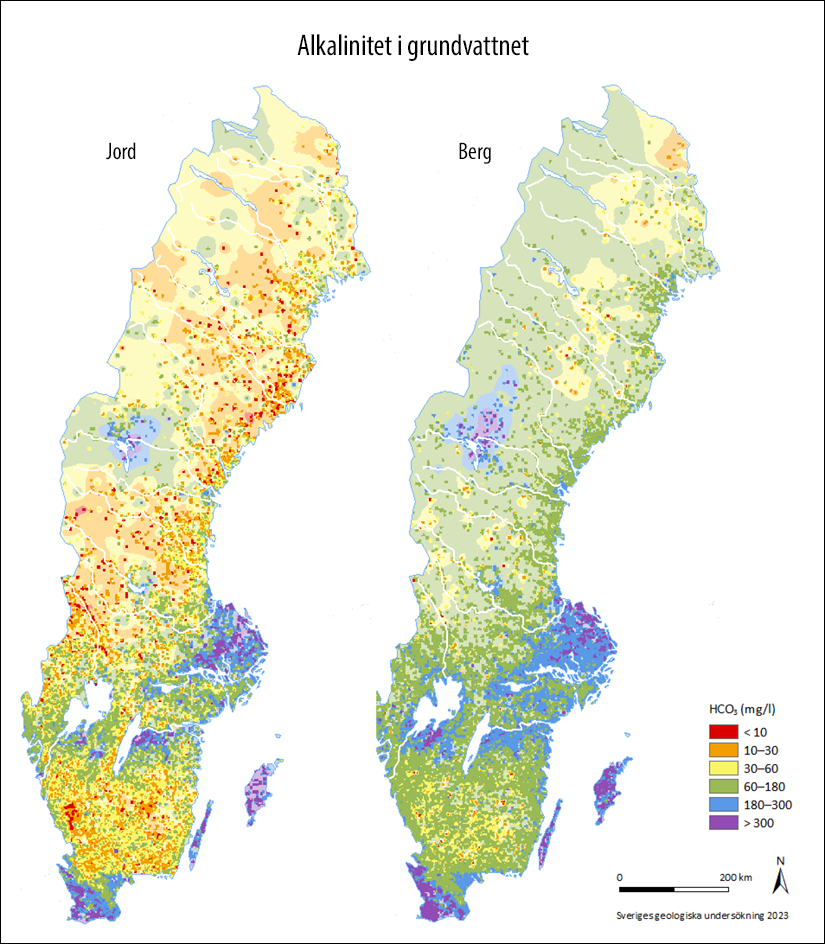
Kartorna visar en generaliserad bild av grundvattenkvaliteten. I stora delar av Sverige är det ont om data, vilket ger större osäkerheter i kartbilden. Detta markeras på kartan med svagare färg. Områden som ligger inom tre kilometer från närmsta provtagningspunkt är markerade med starkare färg.
Läs mer på sidan Vad visar kartorna?
Procentuell fördelning av uppmätta alkalinitetsvärden inom varje kartklassområde
I tabellen visas för varje klass (färg på kartan) vilka halter i grundvattnet som kan förväntas. För klassen större än 180 mg /l (blå och lila områden på kartan) kan exempelvis noteras att 72,3 procent av analyserna från grundvatten i jord har en alkalinitet över 180 mg/l.
HCO3 |
Grundvatten i jord |
|
|
|
Grundvatten i berg |
|
|
|
||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
|
Uppmätta halter, mg/l |
|
|
Antal analyser |
Uppmätta halter, mg/l |
|
|
Antal analyser |
||||
|
|
>180 |
60–180 |
30–60 |
10–30 |
≤10 |
|
>180 |
60–180 |
30–60 |
10–30 |
≤10 |
|
|
Kartklass |
% |
|
% |
|
||||||||
|
> 180 |
72,3 |
19,5 |
4,5 |
2,4 |
1,4 |
4 509 |
74,3 |
22,9 |
1,6 |
0,6 |
0,6 |
23 221 |
|
60–180 |
18,1 |
38,8 |
21,3 |
17,5 |
4,3 |
7 627 |
21,5 |
62,4 |
9,5 |
4,8 |
1,8 |
21 838 |
|
30–60 |
2,5 |
23,5 |
27,9 |
36,4 |
9,7 |
6 902 |
3,8 |
51,5 |
25,8 |
15,2 |
3,6 |
1 715 |
|
10–30 |
1,2 |
12,6 |
22,7 |
46,0 |
17,5 |
4 359 |
5,0 |
36,1 |
20,8 |
31,2 |
6,9 |
202 |
|
≤ 10 |
1,5 |
10,0 |
11,1 |
31,9 |
45,6 |
270 |
8,3 |
50,0 |
33,3 |
8,3 |
0,0 |
12 |
| Alla | 20,6 |
25,5 |
20,2 |
25,5 |
8,2 |
23 667 |
46,9 |
42,4 |
6,2 |
3,2 |
1,3 |
46 988 |
Bakgrundshalter
Det är svårt att fastställa vilka nivåer på alkalinitet och pH som är naturliga och som skulle ha rått om inte den kraftiga försurningen under 1900-talet hade ägt rum. Markens naturliga produktion av kolsyra har resulterat i en långsam försurning av marken sedan istiden. I det ytliga grundvattnet i jord kan alkaliniteten vara låg, medianvärdet vid den nationella miljöövervakningen är 36 mg/l och 10:e percentilen är 5,8 mg/l [9]. När vattnet perkolerar ner till grundvattnet höjs alkaliniteten successivt genom vittring av markmineral, vilket producerar alkalinitet. Vittringsprocesserna fortsätter i grundvattenzonen. Grundvattnets alkalinitet och pH ökar därmed med tiden och djupet i grundvattnet.
Vittring är beroende av tillförsel av koldioxid och kolsyra, det spelar därför roll om vittringen äger rum i marken, i den omättade zonen ovanför grundvattenytan, eller nere i grundvattnet. Om vittringen huvudsakligen sker ovanför grundvattenytan där ny kolsyra kan tillföras allteftersom den förbrukas vid vittringsreaktionerna, det vill säga att vittringen sker i ett system som är öppet vad avser CO2, kan alkaliniteten i grundvattnet bli hög även vid måttligt höga pH-värden. Om vittringen däremot sker i grundvattenzonen där ytterligare tillförsel av kolsyra är långsam, det vill säga ett system som är slutet vad avser CO2, så tenderar pH-värdena att bli höga även vid måttligt höga alkalinitetsvärden [10].
Alkaliniteten är naturligt hög i områden med kalk i jordlager eller berggrund, det vill säga främst regionerna A, D, F och H. I övriga regioner är alkaliniteten generellt lägre, även om högre alkalinitet kan uppmätas exempelvis i grundvatten under lera eller berggrundvatten med lång uppehållstid. Alkaliniteten begränsas ofta av lösligheten av kalcit (kalciumkarbonat). I områden med stora mängder natrium adsorberade i sediment kan jonbyte, där kalcium i grundvattnet ersätts av natrium, dock medföra mycket höga alkalinitetsvärden eftersom kalcitutfällning förhindras.
Läs mer i avsnitt Indelning i regioner
Påverkanskällor
Mark och grundvatten kan försuras genom kvävetillförsel, om kvävet inte tas upp fullständigt av vegetationen. Utvecklingen av minskningen av nedfall av kväve har inte varit lika god som för svavel, men den tidigare ökande trenden har bytts mot en sjunkande trend som planat ut sedan 1995.
Tillförsel av kväve (framför allt i form av ammonium) vid intensivgödsling och ungskogsgödsling kan ge påtaglig lokal försurningspåverkan i alkalinitetsklass 4 och 5, om tillfört kväve inte tas upp helt av vegetationen och ammonium omvandlas till nitrat. Detta är en försurande process som snabbt kan påverka grundvattnet. Vid kvävegödsling av skogsmark med ammoniumnitrat tillsätts kalk för att minska försurningseffekten i marken. Neutraliseringen genom tillsatsen av kalk är relativt långsam och kommer framför allt markens övre delar till godo. Intensifieringen av skogsbruket med helträdsutnyttjande bedöms dock generellt innebära en större risk för försurningspåverkan än kvävegödsling.
Lokalt kan oxidation av sulfider ge extremt sura vatten med låg eller obefintlig alkalinitet. Oxidation av sulfider i organiska jordarter och i rester från gruvbrytning äger rum när de utsätts för syre. Dränering av sulfidhaltig mark kan således ge sura vatten med hög sulfathalt. Detta gäller i synnerhet så kallade svartmockor [12]. I områden där sulfidmalmer har brutits kan varphögar och annat material ge upphov till extremt sura vatten med höga sulfathalter [13]. Liknande påverkan har kunnat ses i krossat berg med sulfider exempelvis från tunneldrivning (entreprenadberg). Även avsänkning av grundvattenytan i områden med tunna jordtäcken med inslag av myrmarker kan ge ett surare vatten. Detta gäller även uttag av vatten ur berggrunden där dessutom uttagen ger en ökad grundvattenbildning till berggrunden, vilket medför kortare uppehållstider och därigenom kortare tider för att vittringsprocesser ska kunna neutralisera det sura vattnet. Om grundvattenuttaget upphör återgår grundvattnets kemiska sammansättning så småningom till den ursprungliga [14].
Bedömning av tillstånd
pH-mätningar i grundvatten är behäftade med mycket stor osäkerhet. Det är därför bättre att använda alkaliniteten för att bedöma ett grundvattens tillstånd avseende försurning. Vätekarbonatjoner (HCO3–) bidrar absolut mest till alkaliniteten. Alkalinitet är en robust parameter som vanligen inte förändras mellan provtagning och analys. Undantagsvis kan oxidation och utfällning av metaller i grundvattnet leda till sänkt alkalinitet och pH vid kontakt med luftens syre. I områden där grundvattnet är nära mättnad avseende kalciumkarbonat (kalcit) kan de förändrade betingelserna när vattnet lämnar grundvattnet leda till kalkutfällning, och därmed sänkt alkalinitet. I Sverige bestäms alkalinitet vanligen genom titrering med syra ner till pH-värdet 5,4. Om pH-värdet är lägre än 5,4 kan i stället aciditeten bestämmas genom att titrera upp till pH 5,4 med en bas. Aciditet benämns ibland negativ alkalinitet. Vatten med aciditet klassas således i tillståndsklass 5.
Ett annat närliggande mått på den syraneutraliserande förmågan är acid neutralizing capacity (ANC) som utgör skillnaden mellan baskatjoner och de starka syrornas anjoner.
ANC = (Ca + Mg + Na + K) – (SO4 + Cl + NO3)
ANC är därmed mer väldefinierat än alkalinitet och har använts bland annat för modellering och bedömning av försurning av ytvatten [15]. För grundvatten är alkalinitet ofta en huvudkomponent och det är värdefullt att ha en självständig bestämning av denna parameter, i stället för att vara beroende av att alla ingående komponenter i ANC är korrekt bestämda.
Grundvattnets tillstånd vad avser motståndskraft mot försurning bedöms utifrån vattnets alkalinitet i fem klasser. Alkalinitet anges ibland i enheten mekv/l (där 1 mekv/l motsvarar 61 mg/l HCO3).
| Klass | Tillstånd | Alkalinitet (HCO3 mg/l) | Kommentar |
|---|---|---|---|
|
1 |
Mycket hög halt |
> 180 |
Tillräcklig alkalinitet för att bibehålla acceptabel pH-nivå. |
|
2 |
Hög halt |
60–180 |
|
|
3 |
Måttlig halt |
30–60 |
Otillräcklig alkalinitet för att ge stabil och acceptabel pH-nivå. |
|
4 |
Låg halt |
10–30 |
|
|
5 |
Mycket låg halt |
≤ 10 |
Alkaliniteten ger oacceptabel pH-nivå. |
Grundvattnets alkalinitet – indelning efter provtagningsplats och fördelning i procent.
| Klass | 1 | 2 | 3 | 4 | 5 | |
|---|---|---|---|---|---|---|
|
Alkalinitet, HCO3 (mg/l) |
|
> 180 |
60–180 |
30–60 |
10–30 |
≤ 10 |
|
|
Antal |
|
% |
|
|
|
|
Större vattentäkt i jord |
2 111 |
18,6 |
33,2 |
22,5 |
23,6 |
2,2 |
|
Enskild brunn i jord |
24 559 |
22,2 |
27,3 |
20,4 |
23,6 |
6,6 |
|
Källa i jord |
2 571 |
9,9 |
16,3 |
18,6 |
36,5 |
18,7 |
|
Rör i jord |
265 |
17,4 |
29,1 |
17,0 |
15,8 |
20,8 |
|
Större vattentäkt i berg |
1 107 |
34,3 |
51,8 |
9,9 |
3,6 |
0,4 |
|
Enskild brunn i berg |
54 502 |
46,9 |
42,7 |
6,1 |
3,2 |
1,2 |
|
Provpunkter – jord |
29 550 |
20,8 |
26,7 |
20,3 |
24,7 |
7,5 |
|
Provpunkter – berg |
55 610 |
46,7 |
42,9 |
6,1 |
3,2 |
1,1 |
|
Alla provpunkter |
88 679 |
37,8 |
37,2 |
11,1 |
10,6 |
3,3 |
Resultatet baseras på data i SGU:s databaser 2023.
Halter i dricksvatten
Livsmedelsverket anger för alkalinitet 50–150 mg/l HCO3 som ett vägledande riktvärde i utgående vatten från ledningsnät för att minska korrosion. Dessa nivåer behövs för att balansera höga klorid- och sulfathalter, och för att motverka kvalitetsförändringar vid långa uppehållstider [16].
För enskild vattenförsörjning anger Livsmedelsverket inga riktvärden för alkalinitet, men uppger att en viss alkalinitet i vattnet är bra. Halter över 60 mg/l HCO3 minskar risken för att ledningar och annan utrustning i dricksvattenanläggningen angrips och fräts sönder (korroderar) av vattnet. Låg alkalinitet (under 60 mg per liter) kan därför vara orsak till att vattnet innehåller höga halter av metaller, till exempel koppar [17], [18].
Många brunnsvatten i Sverige uppnår inte dessa krav. För att undvika omfattande ledningskorrosion och förhöjda metallhalter bör pH-värdet åtminstone vara högre än 6,0 och helst över 6,5, vilket innebär att alkaliniteten åtminstone bör vara högre än 30 mg/l (0,5 mekv/l). Bergborrade brunnar har vanligen högre alkalinitet än brunnar i jordlagren.
Påverkan på ytvatten
Grundvatten bidrar med alkalinitet till sjöar och vattendrag. Detta tillskott är viktigt för att stabilisera pH-värdet i anslutande ytvatten. Alkaliniteten i ytvatten är generellt mycket lägre än alkaliniteten i ytligt grundvatten – medianvärdet vid omdrevsprovtagningen i sjöar 2007–2022 är 8,5 mg/l HCO3 (0,14 mekv/l) [19], vilket visar att det främst är det allra ytligaste grundvattnet som dominerar grundvattenflödet till sjöar och vattendrag.
Försurat grundvatten har emellertid bidragit och bidrar i viss mån fortfarande till försurningen av ytvatten. Under slutet av 1900-talet fick utflödet av ett surt grundvatten, med höga halter av aluminium, katastrofala konsekvenser för fiskar och andra organismer i många vattendrag och sjöar i Sverige. I och med att depositionen nu har minskat har försurningstillståndet successivt förbättrats även om många vattendrag, särskilt i sydvästra Sverige, fortfarande är försurade. Återhämtningen i sjöar och vattendrag indikerar att vattenkvaliteten i det ytligaste grundvattnet, som framför allt bidrar till vattnet i sjöar och vattendrag, också har förbättrats. Mätdata från grundvatten visar dock inte på någon tydlig förbättring. Det är sannolikt att grundvattnet även under de kommande decennierna kommer att bidra till att fördröja en fullständig återhämtning i ytvattendrag. Skälen till detta är grundvattnets långa omsättningstider och att försurningstillståndet vad avser pH i skogsmark är ganska oförändrat, vilket innebär att återhämtningen för grundvattnet i inströmningsområden fördröjs.
Tröskelvärde och vända-trend-värde för grundvattenförekomster
Vattnets alkalinitet ingår inte i tröskelvärdeslistan i tabell 1 i bilaga 3 till SGU:s föreskrifter om kartläggning, riskbedömning och klassificering av status (SGU–FS 2023:1). När vattenmyndigheterna fastställer ett tröskelvärde för en parameter i en grundvattenförekomst ska det göras utifrån anvisningar i SGU:s föreskrifter. Parametrar som inte ingår i tröskelvärdeslistan har inga beslut om miljökvalitetsnormer men omfattas av övriga bestämmelser i miljöbalken och annan lagstiftning. Om mänsklig verksamhet leder till halter som kan medföra skada för människors hälsa eller för miljön ska vattenmyndigheten meddela detta till SGU, som vid behov gör ett tillägg till tröskelvärdeslistan.
Vattnets alkalinitet är en parameter som kan användas som stöd vid riskbedömning och statusklassificering av grundvattenförekomster. Om grundvattnets innehåll förändras kan det tyda på mänsklig påverkan. Orsaken till förändringen bör undersökas för att utesluta att denna påverkan även riskerar att påverka grundvattenförekomstens kemiska eller kvantitativa status.
SGU:s föreskrifter om kartläggning, riskbedömning och klassificering av status (SGU–FS 2023:1)
Senast ändrad 2024-02-07